Đề kiển tra học kỳ I môn Hóa học Lớp 9 - Năm học 2020-2021 - Trường PTDTBTTH&THCS Phìn Ngan (có đáp án)
I. Trắc nghiệm ( 2 điểm)
Hãy lựa chọn các đáp án đúng trong các câu sau:
1. Các bazơ không tan là
A. NaOH, Mg(OH)2, Fe(OH)3, Fe2O3. B. Mg(OH)2, Fe(OH)3, H3PO4.
C. NaOH, Mg(OH)2, Fe(OH)3. D. Mg(OH)2, Fe(OH)3, Cu(OH)2
2. Dung dịch muối FeCl2 lẫn tạp chất là CuCl2 . Chất có thể làm sạch muối sắt là:
A. AgNO3 ; B. Fe C. Mg ; D. Al ;
3. Dãy kim loại được xếp theo chiều tính kim loại tăng dần là :
A. K , Na , Al , Fe B. Cu, Zn, Fe, Mg
C. Fe , Mg, Na, K D. Ag, Cu, Al , Fe
4. Điều chế nhôm theo cách nào dưới đây?
A. Dùng than chì để khử Al2O3 ở nhiệt độ cao.
B. Điện phân dung dịch muối nhôm.
C. Điện phân Al2O3 nóng chảy.
D. Dùng kim loại Na đẩy Al ra khỏi dung dịch muối nhôm.
II. Tự luân ( 8 điểm)
Câu 1(3 điểm). Hoàn thành các PTHH biểu diễn dãy biến hoá sau :
Al Al2O3 Al2(SO4)3 AlCl3 Al(NO3)3
Al(OH)3 Al2O3
Câu 2. ( 2 điểm). PISA. Tính chất của phi kim
Các nguyên tố phi kim có nhiều trong tự nhiên. Phi kim tồn tại ở cả 3 trạng thái: rắn, lỏng, khí; phần lớn các phi kim không dẫn điện, dẫn nhiệt. Chúng tác dụng được với kim loại, hiddro và oxi. Nhờ những tính chất đó mà phi kim có nhiều ứng dụng trong thực tiễn.
Có 3 khí đựng riêng biệt trong 3 lọ khí: Clo, hiđro clorua và oxi. Hãy nêu phương pháp hóa học để nhận biết từng khí trong mỗi lọ.
Câu 3. ( 3 điểm). Đốt cháy 5,6g Fe trong khí clo dư.
a. Viết PTHH của phản ứng xảy ra.
b. Tính khối lượng muối tạo thành.
c. Hòa tan lượng muối trên bằng 100ml nước. Tính nồng độ mol của dung dịch thu được?
( Biết thể tích dd sau hòa tan là không đổi. Fe = 56, Cl = 35,5)
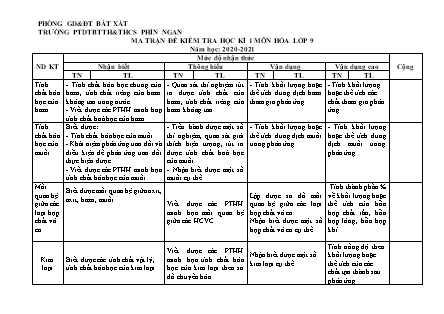
PHÒNG GD&ĐT BÁT XÁT TRƯỜNG PTDTBTTH&THCS PHÌN NGAN MA TRẬN ĐỀ KIỂM TRA HỌC KÌ 1 MÔN HÓA LỚP 9 Năm học: 2020-2021 ND KT Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng Vận dụng cao TN TL TN TL TN TL TN TL Tính chất hóa học của bazơ - Tính chất hóa học chung của bazơ, tính chất riêng của bazơ không tan trong nước. - Viết được các PTHH minh hoạ tính chất hoá học của bazơ. - Quan sát thí nghiệm rút ra được tính chất của bazơ, tính chất riêng của bazơ không tan. - Tính khối lượng hoặc thể tích dung dịch bazơ tham gia phản ứng. - Tính khối lượng hoặc thể tích các chất tham gia phản ứng. Tính chất hóa học của muối Biết được: - Tính chất hóa học của muối - Khái niệm phản ứng trao đổi và điều kiện để phản ứng trao đổi thực hiện được. - Viết được các PTHH minh họa tính chất hóa học của muối. - Tiến hành được một số thí nghiệm, quan sát giải thích hiện tượng, rút ra được tính chất hoá học của muối. - Nhận biết được một số muối cụ thể. - Tính khối lượng hoặc thể tích dung dịch muối trong phản ứng. - Tính khối lượng hoặc thể tích dung dịch muối trong phản ứng. Mối quan hệ giữa các loại hợp chất vô cơ Biết được mối quan hệ giữa oxit, axit, bazơ, muối. Viết được các PTHH minh họa mối quan hệ giữa các HCVC Lập được sơ đồ mối quan hệ giữa các loại hợp chất vô cơ. Nhận biết được một số hợp chất vô cơ cụ thể. Tính thành phần % về khối lượng hoặc thể tích của hỗn hợp chất rắn, hỗn hợp lỏng, hỗn hợp khí. Kim loại Biết được các tính chất vật lý, tính chất hóa học của kim loại Viết được các PTHH minh họa tính chất hóa học của kim loại theo sơ đồ chuyển hóa Nhận biết được một số kim loại cụ thể Tính nồng độ theo khối lượng hoặc thể tích của các chất tạo thành sau phản ứng. PHÒNG GD&ĐT BÁT XÁT TRƯỜNG PTDTBTTH&THCS PHÌN NGAN BẢNG MÔ TẢ MÔN KIỂM TRA HỌC KÌ I - MÔN HÓA 9 NĂM HỌC 2020 - 2021 I. Trắc nghiệm Câu 1(2,0 đểm): Dạng câu hỏi có 1 lựa chọn, điền khuyết, đúng/ sai. - Yêu cầu xác định được tính chất hóa học chung của bazơ, tính chất riêng của bazơ không tan trong nước. Viết được các PTHH minh hoạ tính chất hoá học của bazơ. - Biết được: Tính chất hóa học của muối. Khái niệm phản ứng trao đổi và điều kiện để phản ứng trao đổi thực hiện được.Viết được các PTHH minh họa tính chất hóa học của muối. - Biết được: Mối quan hệ giữa các loại hợp chất vô cơ, viết được các PTHH minh họa cho mối quan hệ đó. II. Tự luận: Câu 2(3,0 điểm): Viết phương trình Yêu cầu hiểu và viết được phương trình hóa học theo sơ đồ chuyển hóa hoặc hoàn thành phương trình hóa học về kim loại, bazơ, muối (viết đúng, đảm bảo chính xác, đủ điều kiện). Câu 3(2,0 điểm): Nhận biết Vận dụng kiến thức đã học về tính chất vật lí, hóa học của kim loại, tính chất hóa học của bazơ, muối nhận biết kim loại hoặc axit, bazơ và muối. Câu 4(3,0 điểm): Bài tập tính toán Hiểu được tính chất hóa học của kim loại và vận dụng vào viết phương trình, giải bài tập tính số mol, khối lượng, nồng độ dung dịch. PHÒNG GD&ĐT BÁT XÁT ĐỀ KIỂM TRA HỌC KÌ I Trường PTDTBTTH&THCS PHÌN NGAN Đề 1 Năm học 2020 - 2021 Môn: Hóa học lớp 9 Thời gian: 45 phút I. Trắc nghiệm ( 2 điểm) Hãy lựa chọn các đáp án đúng trong các câu sau: 1. Các bazơ không tan là A. NaOH, Mg(OH)2, Fe(OH)3, Fe2O3. B. Mg(OH)2, Fe(OH)3, H3PO4. C. NaOH, Mg(OH)2, Fe(OH)3. D. Mg(OH)2, Fe(OH)3, Cu(OH)2 2. Dung dịch muối FeCl2 lẫn tạp chất là CuCl2 . Chất có thể làm sạch muối sắt là: A. AgNO3 ; B. Fe C. Mg ; D. Al ; 3. Dãy kim loại được xếp theo chiều tính kim loại tăng dần là : A. K , Na , Al , Fe B. Cu, Zn, Fe, Mg C. Fe , Mg, Na, K D. Ag, Cu, Al , Fe 4. Điều chế nhôm theo cách nào dưới đây? A. Dùng than chì để khử Al2O3 ở nhiệt độ cao. B. Điện phân dung dịch muối nhôm. C. Điện phân Al2O3 nóng chảy. D. Dùng kim loại Na đẩy Al ra khỏi dung dịch muối nhôm. II. Tự luân ( 8 điểm) Câu 1(3 điểm). Hoàn thành các PTHH biểu diễn dãy biến hoá sau : AlAl2O3Al2(SO4)3AlCl3Al(NO3)3 Al(OH)3 Al2O3 Câu 2. ( 2 điểm). PISA. Tính chất của phi kim Các nguyên tố phi kim có nhiều trong tự nhiên. Phi kim tồn tại ở cả 3 trạng thái: rắn, lỏng, khí; phần lớn các phi kim không dẫn điện, dẫn nhiệt. Chúng tác dụng được với kim loại, hiddro và oxi. Nhờ những tính chất đó mà phi kim có nhiều ứng dụng trong thực tiễn. Có 3 khí đựng riêng biệt trong 3 lọ khí: Clo, hiđro clorua và oxi. Hãy nêu phương pháp hóa học để nhận biết từng khí trong mỗi lọ. Câu 3. ( 3 điểm). Đốt cháy 5,6g Fe trong khí clo dư. a. Viết PTHH của phản ứng xảy ra. b. Tính khối lượng muối tạo thành. Hòa tan lượng muối trên bằng 100ml nước. Tính nồng độ mol của dung dịch thu được? ( Biết thể tích dd sau hòa tan là không đổi. Fe = 56, Cl = 35,5) ---------*****---------- ĐÁP ÁN – HƯỚNG DẪN CHẤM ĐỀ 1 I. Trắc nghiệm (2 điểm) Mỗi đáp án đúng 0,5 điểm 1. D 2. B 3. C 4. C II. Tự luận (8 điểm) Câu 1 (3 điểm). Mỗi ý đúng: 0,5 điểm 1. 4Al + 3O2 2Al2O3 2. Al2O3 + 3H2SO4 Al2(SO4)3 + 3H2O 3. Al2(SO4)3 + 3BaCl2 3BaSO4 + 2AlCl3 4. AlCl3 + 3AgNO3 Al(NO3)3 + 3 AgCl 5. Al(NO3)3 + 3 NaOH Al(OH)3 + 3 NaNO3 6. 2Al(OH)3 Al2O3 + 3H2O ( Lưu ý: HS viết đúng sơ đồ PƯ được 0,25 điểm, cân bằng đúng được 0,25 điểm) Câu 2. (2 điểm). - Dẫn các khí trên vào 3 cốc nước có chứa mẩu giấy quỳ tím sau đó quan sát. 0,5 - Khí nào làm mẩu quỳ tím đổi màu thành đỏ là khí HCl. 0,5 - Khí nào làm mẩu quỳ tím đổi màu thành đỏ sau đó mất màu là khí Cl2. 0,5 - Khí nào không thấy có hiện tượng gì khí đó là khí O2. 0,5 Câu 3. (3 điểm) - Mức đầy đủ: Hs trả lời đúng và đủ được điểm tối đa: a. PTHH của phản ứng: 2Fe + 3Cl2 2 FeCl3 0,5 - Theo đầu bài ta có: nFe = 0,5 - Theo PTHH ta có: 0,5 - Khối lượng của muối tạo thành là: 0,5 c. Theo đầu bài ta có: 0,5 Nồng độ mol của dd sau khi pha là: 0,5 - Mức chưa đầy đủ: Hs trả lời thiếu hoặc sai ý nào trừ điểm ý đó - Mức chưa đạt: Hs không trả lời hoặc trả lời sai không cho điểm ( Lưu ý: HS làm bài tập theo cách khác nếu đúng được điểm tối đa) Ngày .. .. Ngày Tổ chuyên môn duyệt Ban giám hiệu duyệt PHÒNG GD&ĐT BÁT XÁT ĐỀ KIỂM TRA HỌC KÌ I Trường PTDTBTTH&THCS PHÌN NGAN Đề 2 Năm học 2020 - 2021 Môn: Hóa học 9 Thời gian: 45 phút I. Trắc nghiệm ( 2 điểm) Hãy lựa chọn các đáp án đúng trong các câu sau: 1. Dãy kim loại được xếp theo chiều tính kim loại tăng dần là : A. K , Na , Al , Fe B. Cu, Zn, Fe, Mg C. Fe , Mg, Na, K D. Ag, Cu, Al , Fe 2. Các bazơ không tan là A. NaOH, Mg(OH)2, Fe(OH)3, Fe2O3. B. Mg(OH)2, Fe(OH)3, H3PO4. C. NaOH, Mg(OH)2, Fe(OH)3. D. Mg(OH)2, Fe(OH)3, Cu(OH)2 3. Điều chế nhôm theo cách nào dưới đây? A. Dùng than chì để khử Al2O3 ở nhiệt độ cao. B. Điện phân dung dịch muối nhôm. C. Điện phân Al2O3 nóng chảy. D. Dùng kim loại Na đẩy Al ra khỏi dung dịch muối nhôm. 4. Dung dịch muối FeCl2 lẫn tạp chất là CuCl2 . Chất có thể làm sạch muối sắt là: A. AgNO3 ; B. Fe C. Mg ; D. Al ; II. Tự luân ( 8 điểm) Câu 1(3 điểm). Hoàn thành các PTHH biểu diễn dãy biến hoá sau : Fe(OH)3 Fe2O3 Fe FeCl3 Fe(NO3)3 Fe(OH)3 Fe2(SO4)3 Câu 2. ( 2 điểm). PISA. Tính chất của phi kim Các nguyên tố phi kim có nhiều trong tự nhiên. Phi kim tồn tại ở cả 3 trạng thái: rắn, lỏng, khí; phần lớn các phi kim không dẫn điện, dẫn nhiệt. Chúng tác dụng được với kim loại, hiddro và oxi. Nhờ những tính chất đó mà phi kim có nhiều ứng dụng trong thực tiễn. Có 3 khí đựng riêng biệt trong 3 lọ khí: Clo, hiđro clorua và oxi. Hãy nêu phương pháp hóa học để nhận biết từng khí trong mỗi lọ. Câu 3. ( 3 điểm). Đốt cháy 2,7 gam Al trong khí clo dư. a. Viết PTHH của phản ứng xảy ra. b. Tính khối lượng muối tạo thành. Hòa tan lượng muối trên bằng 100ml nước. Tính nồng độ mol của dung dịch thu được? ( Biết thể tích dd sau hòa tan là không đổi. Al = 27, Cl = 35,5) ---------*****---------- ĐÁP ÁN – HƯỚNG DẪN CHẤM ĐỀ 2 I. Trắc nghiệm (2 điểm) Mỗi đáp án đúng 0,5 điểm 1. C 2. D 3. C 4. B II. Tự luận (8 điểm) Câu 1 (3 điểm). Mỗi ý đúng: 0,5 điểm 1/ 2 Fe(OH)3 Fe2O3 + 3 H2O 2/ Fe2O3 + 3 CO 2 Fe + 3 CO2 3/ 2 Fe + 3Cl2 2 FeCl3 4/ FeCl3 + 3 AgNO3 Fe(NO3)3 + 3 AgCl 5/ Fe(NO3)3 + 3 KOH Fe(OH)3 + 3 KNO3 6/ 2 Fe(OH)3 + 3 H2SO4 Fe2(SO4)3 + 6 H2O ( Lưu ý: HS viết đúng sơ đồ PƯ được 0,25 điểm, cân bằng đúng được 0,25 điểm) Câu 2. (2 điểm). - Dẫn các khí trên vào 3 cốc nước có chứa mẩu giấy quỳ tím sau đó quan sát. 0,5 - Khí nào làm mẩu quỳ tím đổi màu thành đỏ là khí HCl. 0,5 - Khí nào làm mẩu quỳ tím đổi màu thành đỏ sau đó mất màu là khí Cl2. 0,5 - Khí nào không thấy có hiện tượng gì khí đó là khí O2. 0,5 Câu 3. (3 điểm) - Mức đầy đủ: Hs trả lời đúng và đủ được điểm tối đa: a. PTHH của phản ứng: 2Al + 3Cl2 2 AlCl3 0,5 - Theo đầu bài ta có: nAl = 0,5 - Theo PTHH ta có: 0,5 - Khối lượng của muối tạo thành là: 0,5 c. Theo đầu bài ta có: 0,5 Nồng độ mol của dd sau khi pha là: 0,5 - Mức chưa đầy đủ: Hs trả lời thiếu hoặc sai ý nào trừ điểm ý đó - Mức chưa đạt: Hs không trả lời hoặc trả lời sai không cho điểm ( Lưu ý: HS làm bài tập theo cách khác nếu đúng được điểm tối đa) Ngày .. .. Ngày Tổ chuyên môn duyệt Ban giám hiệu duyệt PHÒNG GD&ĐT BÁT XÁT ĐỀ KIỂM TRA HỌC KÌ I Trường PTDTBTTH&THCS PHÌN NGAN Đề dự phòng Năm học: 2020 - 2021 Môn: Hóa học lớp 9 Thời gian: 45 phút I. Trắc nghiệm ( 2 điểm) Hãy lựa chọn các đáp án đúng trong các câu sau: 1. Các bazơ không tan là A. NaOH, Mg(OH)2, Fe(OH)3, Fe2O3. B. Mg(OH)2, Fe(OH)3, H3PO4. C. NaOH, Mg(OH)2, Fe(OH)3. D. Mg(OH)2, Fe(OH)3, Cu(OH)2 2. Dung dịch muối FeCl2 lẫn tạp chất là CuCl2 . Chất có thể làm sạch muối sắt là: A. AgNO3 ; B. Fe C. Mg ; D. Al ; 3. Dãy kim loại được xếp theo chiều tính kim loại tăng dần là : A. K , Na , Al , Fe B. Cu, Zn, Fe, Mg C. Fe , Mg, Na, K D. Ag, Cu, Al , Fe 4. Điều chế nhôm theo cách nào dưới đây? A. Dùng than chì để khử Al2O3 ở nhiệt độ cao. B. Điện phân dung dịch muối nhôm. C. Điện phân Al2O3 nóng chảy. D. Dùng kim loại Na đẩy Al ra khỏi dung dịch muối nhôm. II. Tự luân ( 8 điểm) Câu 1(3 điểm). Hoàn thành các PTHH biểu diễn dãy biến hoá sau : AlAl2O3Al2(SO4)3AlCl3Al(NO3)3 Al(OH)3 Al2O3 Câu 2. ( 2 điểm). PISA. Tính chất của phi kim Các nguyên tố phi kim có nhiều trong tự nhiên. Phi kim tồn tại ở cả 3 trạng thái: rắn, lỏng, khí; phần lớn các phi kim không dẫn điện, dẫn nhiệt. Chúng tác dụng được với kim loại, hiddro và oxi. Nhờ những tính chất đó mà phi kim có nhiều ứng dụng trong thực tiễn. Có 3 khí đựng riêng biệt trong 3 lọ khí: Clo, hiđro clorua và oxi. Hãy nêu phương pháp hóa học để nhận biết từng khí trong mỗi lọ. Câu 3. ( 3 điểm). Cho 10 gam hçn hîp Cu vµ CuO t¸c dông víi dd H2SO4 lo·ng, läc lÊy chÊt r¾n kh«ng tan, cho vµo dung dÞch H2SO4 ®Æc, nãng thu ®îc 1,12 lÝt khÝ A ( ®ktc). a) ViÕt PTHH c¸c ph¶n øng xÈy ra vµ cho biÕt tªn khÝ A? b) TÝnh phÇn tr¨m khèi lîng c¸c chÊt trong hçn hîp? ( Cho biÕt: Cu = 64, O =16, H =1) ---------*****---------- ĐÁP ÁN – HƯỚNG DẪN CHẤM ĐỀ DỰ PHÒNG I. Trắc nghiệm (2 điểm) Mỗi đáp án đúng 0,5 điểm 1. D 2. B 3. C 4. C II. Tự luận (8 điểm) Câu 1 (3 điểm). Mỗi ý đúng: 0,5 điểm 1. 4Al + 3O2 2Al2O3 2. Al2O3 + 3H2SO4 Al2(SO4)3 + 3H2O 3. Al2(SO4)3 + 3BaCl2 3BaSO4 + 2AlCl3 4. AlCl3 + 3AgNO3 Al(NO3)3 + 3 AgCl 5. Al(NO3)3 + 3 NaOH Al(OH)3 + 3 NaNO3 6. 2Al(OH)3 Al2O3 + 3H2O ( Lưu ý: HS viết đúng sơ đồ PƯ được 0,25 điểm, cân bằng đúng được 0,25 điểm) Câu 2. (2 điểm). - Dẫn các khí trên vào 3 cốc nước có chứa mẩu giấy quỳ tím sau đó quan sát. 0,5 - Khí nào làm mẩu quỳ tím đổi màu thành đỏ là khí HCl. 0,5 - Khí nào làm mẩu quỳ tím đổi màu thành đỏ sau đó mất màu là khí Cl2. 0,5 - Khí nào không thấy có hiện tượng gì khí đó là khí O2. 0,5 Câu 3. (3 điểm) - Mức đầy đủ: Hs trả lời đúng và đủ được điểm tối đa: Sè mol cña H2 lµ: n = 0,5 điểm Ph¬ng tr×nh: CuO + H2SO4(lo·ng) CuSO4 + H2O 0,5 điểm Cu + 2 H2SO4(®Æc) CuSO4 + H2O + SO2 0,5 điểm 0,05 0,05(mol) 0,25 điểm A lµ khÝ lu huúnh dioxit SO2 0,25 điểm mCu = 64. 0,05 = 3,2(g) 0,5 điểm % Cu = 3,2/ 10 x 100 = 32% 0,25 điểm % MgO = 100 – 32 = 68% 0,25 điểm - Mức chưa đầy đủ: Hs trả lời thiếu hoặc sai ý nào trừ điểm ý đó - Mức chưa đạt: Hs không trả lời hoặc trả lời sai không cho điểm ( Lưu ý: HS làm bài tập theo cách khác nếu đúng được điểm tối đa) Ngày .. .. Ngày Tổ chuyên môn duyệt Ban giám hiệu duyệt
Tài liệu đính kèm:
 de_kien_tra_hoc_ky_i_mon_hoa_hoc_lop_9_nam_hoc_2020_2021_tru.docx
de_kien_tra_hoc_ky_i_mon_hoa_hoc_lop_9_nam_hoc_2020_2021_tru.docx



